Wetenschappers hebben hoge verwachtingen van de CRISPR / Cas9-technologie, die zeer nauwkeurige veranderingen in het genoom van levende organismen mogelijk maakt, inclusief mensen. Alle nieuwe wetenschappelijke artikelen worden gepubliceerd waarin verschillende typen CRISPR-systemen worden beschreven, evenals hun wijzigingen. "Lenta.ru" vertelt over de ontdekkingen op dit gebied, gedaan in 2016.
Duizenden
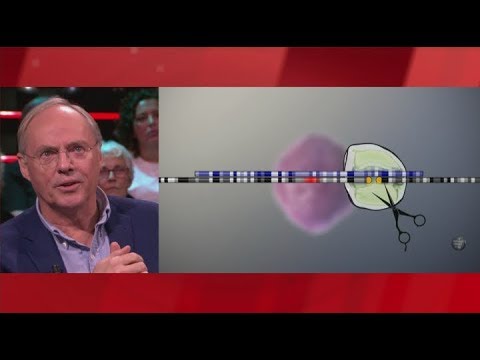
CRISPR / Cas9 is een bacterieel adaptief immuniteitssysteem waarmee micro-organismen virussen kunnen bestrijden. Het bestaat uit spacers - DNA-secties die overeenkomen met bepaalde fragmenten (protospacers) van het DNA van de infectieuze agent. De spacers coderen voor specifieke crRNA-moleculen die binden aan het Cas9-enzym. Het resulterende complex hecht zich aan de DNA-ketting van het virus en Cas9 werkt als een schaar en knipt het door.
In feite is CRISPR / Cas9 slechts een van de vele vergelijkbare systemen die bacteriën en archaea hebben. Wetenschappers verdelen ze in twee klassen. De eerste klasse omvat CRISPR-systemen van type I, III en IV, en de tweede - II en V. Type II bevat het Cas9-eiwit dat betrokken is bij de verwerving van nieuwe spacers, de accumulatie van crRNA in de cel en DNA-splitsing. In andere systemen worden voor deze doeleinden multi-eiwitcomplexen gebruikt. Dit maakt type II het eenvoudigste type CRISPR-systeem dat geschikt is voor genetische manipulatie.
Typen kunnen op hun beurt worden onderverdeeld in subtypen, afhankelijk van welke extra genen zijn geassocieerd met CRISPR. IIA-systemen bevatten bijvoorbeeld het csn2-gen, dat codeert voor een eiwit dat aan DNA bindt en betrokken is bij het verwerven van spacers. In IIB-systemen is csn2 afwezig, maar er is een cas4-gen waarvan de functie nog onbekend is, en IIC-systemen hebben noch csn2 noch cas4.
Schatten in bacteriën
Promotie video:
Alle bekende CRISPR-systemen zijn door wetenschappers ontdekt in bacteriën die in laboratoriumomstandigheden zijn gekweekt. Er is echter een groot aantal niet-gecultiveerde micro-organismen, waaronder zowel archaea als bacteriën. Ze leven meestal in extreme omstandigheden - minerale bronnen of giftige waterlichamen in verlaten mijnen. Onderzoekers kunnen er echter DNA uit isoleren en er specifieke regio's in identificeren. In een nieuw artikel dat op 22 december in Nature werd gepubliceerd, decodeerden genetici van de University of California, Berkeley genomen van natuurlijke microbiële gemeenschappen en ontdekten ze andere variaties van het CRISPR-systeem.
Bacteriofaag - een virus dat bacteriën infecteert

Afbeelding: Giovanni Cancemi / Depositphotos
Wetenschappers zijn erin geslaagd erachter te komen dat sommige soorten weinig bestudeerde arche-achtige nanoorganismen ARMAN ook CRISPR / Cas9 bezitten, hoewel eerder werd aangenomen dat alleen bacteriën ze hebben. Opgemerkt wordt dat dit systeem een tussenliggende plaats inneemt tussen de subtypen IIC en IIB en kan dienen als verdediging tegen parasitaire "springende" genen (transposons) die het micro-organisme binnendringen vanuit andere archaea. Een poging om de activiteit van archaeum CRISPR / Cas9 in E. coli (Escherichia coli) te reproduceren, leidde niet tot iets, wat wijst op het bestaan van enkele aanvullende specifieke mechanismen die het systeem reguleren.
Nieuwe soorten systemen binnen de tweede klasse, CRISPR / CasX en CRISPR / CasY, werden ook geïsoleerd uit bacteriën die in grondwater en sedimenten leven. Het CRISPR / CasX-systeem omvat de eiwitten Cas1, Cas2, Cas4 en CasX. De laatste, zoals aangetoond door experimenten met E. coli, onderscheidt zich door nuclease-activiteit, dat wil zeggen, het is in staat vreemd DNA te splitsen zoals Cas9. Dit gebeurt echter alleen als de TTCN-sequentie vóór de protospacers staat, waarbij N een van de vier nucleotiden is. Dergelijke sequenties worden PAM genoemd (protospacer aangrenzend motief - motief grenzend aan de protospacer). Het CRISPR / Cas9-systeem heeft ook zijn eigen PAM - NGG, die zich na de protospacer zou moeten bevinden. Bovendien is CRISPR / CasY in staat om DNA te knippen als er een TA PAM-sequentie in de buurt van de doellocatie is.
Wat is de belofte van deze ontdekking? Feit is dat de gedetecteerde systemen de meest compacte zijn die op dit moment bekend zijn. Volgens wetenschappers maakt de kleine hoeveelheid eiwitten die nodig zijn voor hun werk CRISPR / CasX en CRISPR / CasY handige tools voor het bewerken van DNA. Bovendien zal metagenomisch onderzoek, waarbij DNA verkregen uit de omgeving wordt bestudeerd, andere typen CRISPR-systemen aan het licht brengen die nuttig zijn voor genetische manipulatie.
De weg naar uitmuntendheid
Er is natuurlijk een alternatief voor het zoeken naar CRISPR-systemen in de natuur - het verbeteren van de reeds bestaande CRISPR / Cas9-technologie. Ondanks haar hoge nauwkeurigheid maakt ze fouten door DNA op de verkeerde plaats te knippen. Dit maakt het moeilijk om de juiste veranderingen in genen aan te brengen en daarmee erfelijke ziekten effectief te behandelen. Daarom zoeken wetenschappers naar manieren om de prestaties van het systeem te verbeteren. In 2016 zijn er veel wetenschappelijke werken geweest die zijn gewijd aan het aanpassen van CRISPR en het omzetten in verschillende gen-tools.
Eiwit Cas9 en crRNA - de belangrijkste componenten van het CRISPR-systeem

Afbeelding: Steve Dixon / Feng Zhang / MIT
Dus publiceerde het tijdschrift Cell op 8 december een artikel van wetenschappers van de Universiteit van Toronto, die "anti-CRISPR" creëerden - een systeem dat het mechanisme onder bepaalde voorwaarden uitschakelt. Hiermee kun je Cas9-activiteit onderdrukken als het gids-RNA aan het verkeerde fragment bindt en fouten voorkomt. Anti-CRISPR is samengesteld uit drie nucleaseremmende eiwitten. Aanvankelijk was het natuurlijk niet uitgevonden door wetenschappers, maar door virussen, die zo de immuniteit van bacteriën neutraliseerden.
In juni bevestigden Amerikaanse onderzoekers, samen met collega's uit Rusland, dat het CRISPR / C2c2-systeem, verkregen uit de fusobacterium Leptotrichia shahii, in staat is om enkelstrengs RNA te snijden. Als gevolg hiervan kan het CRISPR-systeem worden gebruikt om messenger-RNA, dat informatie van genen naar ribosomen overbrengt, uit te schakelen - functies te onderdrukken, waar op basis daarvan eiwitten worden gesynthetiseerd.
In mei creëerden onderzoekers van de University of California de CRISPR-EZ-technologie, waarmee nieuwe DNA-moleculen met bijna honderd procent succes in de genomen van muizenembryo's kunnen worden ingebracht. Het CRISPR / Cas9-systeem wordt met een microscopisch kleine naald en een kleine elektrische ontlading in bevruchte eieren van dieren geïnjecteerd. In hun experiment slaagden wetenschappers erin om bij 88 procent van de muizen een mutatie in een gen te introduceren. Dit overtreft het aantal genetisch gemodificeerde muizen dat wordt geproduceerd door CRISPR-bewerking, waarbij conventionele injecties worden gebruikt.
In april ontwikkelden moleculair biologen van de University of Massachusetts School of Medicine de CRISPRainbow-technologie met behulp van een mutante variant van Cas9 die geen nucleaseactiviteit heeft. Het gids-RNA, dat aangeeft waar de enzymen zich aan hechten, bevatte fluorescerende labels, waardoor het bijvoorbeeld mogelijk is om de beweging van mobiele genetische elementen te volgen.
Anopheles-mug is mogelijk het eerste slachtoffer van CRISPR-systemen

Foto: Jim Gathany / Wikipedia
Dappere nieuwe wereld
Wetenschappers gebruiken CRISPR-systemen al om genetisch gemodificeerde organismen te creëren, zoals de malariamug, die schadelijke genen verspreiden onder hun wilde verwanten. Deze methode heet gene drive. Als een van de ouders van een individu drager was van een mutant gen, dan geeft hij het met een kans van 50 procent door aan zijn nakomelingen. Dit komt doordat de ouder twee exemplaren van het gen heeft en er slechts één defect is. CRISPR kan een mutant fragment kopiëren en in een gezond gen invoegen. Als resultaat krijgen de nakomelingen de mutatie met 100% waarschijnlijkheid.
In 2016 keurden experts van het Recombinant DNA Advisory Committee (RAC) een aanvraag goed van de University of Pennsylvania om tests uit te voeren op menselijke genetische modificatie met behulp van CRISPR / Cas9-technologie.
Ze werden echter ingehaald door de Chinezen. In november meldde het tijdschrift Nature dat Chinese wetenschappers voor het eerst cellen met genen die door het CRISPR / Cas9-systeem waren gemodificeerd, bij mensen introduceerden. De onderzoekers haalden immuuncellen (T-lymfocyten) uit het bloed van een patiënt met uitgezaaide longkanker en gebruikten vervolgens CRISPR-technologie om het gen dat codeert voor het PD-1-eiwit uit te schakelen. Van laatstgenoemde is aangetoond dat het de immuniteit onderdrukt door tumorgroei te bevorderen. Wetenschappers cultiveerden de bewerkte cellen, verhoogden hun aantal en injecteerden ze vervolgens weer in het menselijk lichaam. Of gentherapie de ziekte het hoofd zal bieden, valt nog te bezien.
CRISPR-systemen kunnen ook worden gebruikt om hiv en erfelijke ziekten bij de mens te bestrijden. Er is echter verder onderzoek nodig om effectieve behandelingen te ontwikkelen. We hebben het natuurlijk niet over mutanten, zoals in sciencefictionfilms, maar wetenschappers kunnen snel genetisch gemodificeerde organismen creëren, zoals landbouwgewassen die resistent zijn tegen parasieten. Het valt nog te bezien waarom de wetenschappers die CRISPR hebben ontdekt en erachter zijn gekomen hoe het kan worden gebruikt, nog niet de Nobelprijs hebben ontvangen.
Alexander Enikeev